Дата уроку :27.05.20
Тема уроку: Підсумкова контрольна робота
https://naurok.com.ua/test/start/525762
Чекаю на фотозвіт!!!!!!!
Дата уроку :26.05.20
Тема уроку: Повторення. Атомна та ядерна фізкика.
Домашнє завдання : повторити конспекти з даного розділу.
Дата уроку :25.05.20
Тема уроку: Повторення.Оптика.
Домашнє завдання : повторити конспекти з даного розділу.
Дата уроку :20.05.20
Тема уроку: Повторення. Електромагнітні коливання і хвилі.
Домашнє завдання : повторити конспекти з даного розділу.
Дата уроку : 19.05.20
Тема уроку: Повторення. Постійний електричний струм. Електромагнетизм.
Домашнє завдання : повторити конспекти з даних розділів.
Дата уроку : 18.05.20
Тема уроку: Проект на тему :" Атомна та ядерна фізика "
Домашнє завдання : підготувати проект з даної теми.
Дата уроку : 13.05.20
Тема уроку: Контрольна робота № 5 з теми :"Атомна та ядерна фізика"
Пройти тест та зробити фотозвіт : https://onlinetestpad.com/ua/test/22818-test-z-rozd%D1%96lu-atomna-%D1%96-yaderna-f%D1%96zika
Дата уроку : 12.05.20
Тема уроку:Розв"язування задач. Самостійна робота.

Домашнє завдання: опрацювати тест для самоперевірки.
Дата уроку : 06.05.20


Дата уроку : 05.05.20
Тема уроку: Елементарні частинки. Розв"язування задач.
ЕЛЕМЕНТАРНІ ЧАСТИНКИ, ЇХ КЛАСИФІКАЦІЯ ТА ХАРАКТЕРИСТИКА
Вивчаючи фізику, ми не раз говорили про існування в природі частинок, які називаються елементарними. Ви вже ознайомилися з електроном, фотоном, протоном і нейтроном. Але що ж таке елементарна частинка?
У самому слові елементарна закладено подвійний зміст. З одного боку, елементарний — це найпростіший. З другого боку, під елементарним розуміють щось фундаментальне, що лежить в основі речей (саме в цьому розумінні і називають субатомні частинки (частинки, з яких складаються атоми) елементарними).
Вважати відомі на сьогодні елементарні частинки подібними до незмінних атомів Демокріта не дозволяє такий простий факт. Жодна з частинок не існує вічно. Більшість елементарних частинок не може проіснувати більше від двох мільйонних частинок секунди, навіть тоді, коли немає ніякого зовнішнього впливу. Наприклад, вільний нейтрон (нейтрон поза атомним ядром) існує в середньому 15 хв.
Тільки такі частинки, як фотон, електрон, протон і нейтрино, могли б залишитися незмінними, якби кожна з них була одна на світі.
Але разом з електронами і протонами існують позитрони і антипротони, від зіткнення з якими частинки взаємно знищуються і утворюються нові.

Мал. 218

Мал. 219

Мал. 220
Фотон, випромінений настільною лампою, існує не довше від 10-8 с. Це той час, який йому потрібен, щоб долетіти до сторінки книжки і поглинутися папером.
Лише нейтрино майже вічне, тому що воно надзвичайно слабо взаємодіє з іншими частинками. Але й нейтрино гинуть від зіткнення з іншими частинками, хоч такі зіткнення трапляються рідко. Усі елементарні частинки перетворюються одна в одну, і ці взаємні перетворення — основний факт їх існування.
На мал. 218 ви бачите результат зіткнення ядра Карбону, що мало енергію 60 млрд. еВ (жирна верхня лінія), з ядром Аргентуму фотоемульсії. Ядро розпадається на уламки, які розлітаються в усі боки. Одночасно народжується багато нових елементарних частинок — піонів.
За сучасними уявленнями елементарні частинки — це первинні частинки, які далі не розкладаються, — з них складається вся матерія. Проте неподільність елементарних частинок не означає, що вони не мають внутрішньої структури.
Існування двійника електрона—позитрона — теоретично передбачив англійський фізик П. Дірак у 1931 р. Коли зустрічаються позитрон і електрон, обидві частинки зникають — анігілюють, народжуючи фотони великої енергії. Може бути і зворотний процес — утворення електронно-позитронної пари, наприклад, коли стикається фотон досить великої енергії (його маса має бути більшою від суми мас спокою народжуваних частинок) з ядром.
Через два роки позитрон виявили за допомогою камери Вільсона, вміщеної в магнітне поле. Напрям викривлення треку частинки вказував на знак її заряду, а за радіусом кривизни й енергією частинки визначили відношення її заряду до маси. Воно за значенням таке саме, як і для електрона. На мал. 219 ви бачите першу фотографію, яка довела існування позитрона. Частинка рухалася вгору і, пройшовши через свинцеву пластинку, втратила частину своєї енергії. Тому кривизна траєкторії збільшилась.
Процес утворення пари електрон—позитрон у-квантом у свинцевій пластинці — видно на фотографії, поданій на мал. 220. У камері Вільсона, вміщеній у магнітне поле, пара залишає характерний слід у вигляді дворогої вилки.
Те, що зникнення одних частинок і поява інших під час реакції між елементарними частинками — це перетворення, а не просто виникнення нової комбінації складових частин старих частинок, особливо наочно виявляється саме під час анігіляції пари електрон—позитрон. Обидві ці частинки мають певну масу в стані спокою — електричні заряди.
Порівняно недавно виявили антипротон і антинейтрон. Електричний заряд антипротона негативний.
Атоми, ядра яких складаються з анти нуклоні в, а оболонка — з позитронів, утворюють антиречовину. У 1969 р. уперше було одержано антигелій.
Під час β-розпаду з ядра вилітає електрон. Але електрона в ядрі немає. Звідки ж він береться? Після того як електрон вилітає з ядра, заряд ядра, а отже, і кількість протонів збільшується на одиницю. Масове число ядра не змінюється. Це означає, що кількість нейтронів зменшується на одиницю. Отже, у β-радіоактивних ядрах нейтрон здатний розпадатися на протон і електрон. Протон залишається в ядрі, а електрон вилітає назовні. Лише в стабільних ядрах нейтрони стійкі.
Швейцарський фізик В. Паулі припустив, що разом з протоном і електроном під час розпаду нейтрона народжується якась частинка-«невидимка», що й виносить із собою енергію, якої не вистачає. Цю частинку прилади не реєструють, оскільки вона не має електричного заряду і маси спокою. Отже, вона не може йонізувати атоми, розщеплювати ядра, тобто не може спричинювати ефекти, за якими можна судити про виникнення частинки.
Цю частинку Фермі назвав нейтрино, що означає «нейтрончик». Виявилось, що маса спокою нейтрино, як і передбачав Паулі, дорівнює нулю. За цими словами ховається простий зміст: нейтрино в стані спокою немає. Ледь з’явившись на світ, вони одразу рухаються зі швидкістю 300 000 км/с. Розраховуючи взаємодію нейтрино з речовиною в шарі певної товщини, одержали досить невтішний результат щодо можливості виявити цю частинку експериментально. Земна куля для нейтрино прозоріша, ніж найкраще скло для світла.
Роль нейтрино не зводиться лише до пояснення β-розпаду ядер. Багато елементарних частинок у вільному стані спонтанно розпадається, випромінюючи нейтрино. Передусім так поводиться нейтрон. Тільки у ядрах нейтрон внаслідок взаємодії з іншими нуклонами набуває стабільності. Вільний нейтрон живе в середньому 15 хв. Це довели експериментально лише після того, як було побудовано ядерні реактори, що дають потужні пучки нейтронів.
Як і інші частинки, нейтрино v має античастинку, яка називається антинейтрино — v. Під час розпаду нейтрона на протон і електрон випромінюється саме антинейтрино:
n - р + е- + v .
Енергія нейтрона завжди більша від суми енергій протона й електрона. Надлишкову енергію виносить із собою антинейтрино.
Розпад частинки — зовсім не ознака того, що вона не елементарна. Нейтрон, незважаючи на свою нестабільність, вважається елементарною частинкою, а дейтрон, без сумніву, складається з нейтрона і протона, хоч він і стабільний.
Відкриття нової елементарної частинки завжди було і зараз є визначним тріумфом науки. Але вже давно до кожного чергового тріумфу почало домішуватися занепокоєння. Оскільки тріумфи відбувалися буквально один за одним.
Було відкрито групу «дивних» частинок: К-мезонів і гіперонів з масами, більшими від маси нуклонів. У 70-ті роки XX ст. до них приєдналася велика група «зачарованих» частинок, які мають ще більші маси. Крім того, було відкрито частинки з коротким життям — порядку 10-22 - 10-23 с. Ці частинки назвали резонансами: їх було більше 200.
Якщо до таблиці елементарних частинок не вносити резонанси і «зачаровані» частинки, то матимемо 39 частинок.
Усі частинки поділяються на групи:
1. Фотон.
2. Лептони. Сюди входять 12 частинок (з античастинками). Є 3 види нейтрино: електронне нейтрино народжується разом з електронами, мюонне нейтрино —з -мезонами і r-мезонне нейтрино —з μ-мезонами. Далі йдуть електрон, μ -мезон і r-мезон, відкритий у 1975 р. Хоча μ-мезон має дуже велику масу, він входить до групи лептонів, тому за всіма іншими властивостями він до них близький. Основна властивість, яка споріднює його з лептонами, полягає в тому, що ця частинка, як і інші лептони, не бере участі в сильних взаємодіях. Що ж до r-мезонного нейтрино, то його експериментально поки не виявлено, хоч сумніву в його існуванні немає.
3. Мезони. Ця група має 8 частинок. Найлегші з них 7С-мезони: позитивні, негативні й нейтральні. їх маси становлять 264 (п°) і 273(п+, п-) електронних мас. Піони — це кванти ядерного поля, подібно до того, як фотони є квантами електромагнітного поля. Ще є 4 К-мезони і один η°-мезон.
4. Баріони. До цієї групи входять 18 частинок із 39. Найлегші баріони — це протони і нейтрони. За ними йдуть так звані гіперони. Таблицю замикає Ω- (омега мінус)-частинка, відкрита у 1964 р. Її маса в 3273 рази більша від маси електрона.
Існування великої кількості частинок наводить на думку, що не всі вони однаково елементарні.
Ще в 1963 p. М. Гелл-Манн і Дж. Цвейг запропонували модель, за якою всі частинки, що беруть участь у сильних (ядерних) взаємодіях, народжених
з фундаментальніших (або первинних) частинок — кварків. Крім фотонів і лептонів, усі інші відкриті на сьогодні частинки є складними.
Спочатку було висловлено гіпотезу про існування трьох кварків (і відповідно трьох антикварків). Кваркам приписувалися дробові електричні заряди, їх позначають літерами: и, d, s. Перший — ц-кварк — має заряд 2/3 е, a d- і s-кварк мають однакові заряди по -1/3 е (де е — модуль заряду електрона). Протон складається з двох u-кварків і одного d-кварка; піони складаються з комбінації кварк—антикварк і т. д. Дивні частинки (каони і гіперони) містять важчий s-кварк; його називають «дивним».
Передбачалося існування четвертого с-кварка; його назвали «зачарованим». Потім експериментально виявили частинки, до яких входить цей кварк. Маса с-кварка більша від маси s-кварка.
Досліди з розсіюванням нейтрино і електронів надвисоких енергій на нуклонах підтвердили кваркову структуру і протонів, і нейтронів. Але розщепити на кварки нуклони не вдалося.
Кварки шукали і шукають серед материкових порід, відкладень на дні океану, в місячному ґрунті. Але вільних кварків не виявлено.
Очевидно, міжкваркові сили з відстанню не зменшуються, як усі інші, а збільшуються. Якщо це так, то розщепити нуклони та інші частинки на кварки не вдасться ніколи. Протон та інші частинки мають складну структуру, але розщепити їх на частини не можна.
За сучасними уявленнями, всі лептони, як і кварки, не мають внутрішньої структури. У цьому розумінні лептони і кварки можна вважати справді елементарними частинками. Без античастинок відкрито шість лептонів. Відкрито п’ять кварків. П’ятий — це так званий 6-кварк, маса якого більша від маси с-кварка. Припускають, що є ще й шостий кварк, масивніший за 6-кварк. Теоретичний аналіз приводить до висновку про те, що має бути кварк- лептонна симетрія: речовина, побудована з шести різних лептонів і шести різних кварків. Разом з їх античастинками цих справжніх елементарних частинок налічується 24.
До них треба ще додати квант електромагнітного поля — фотон — і кванти поля, що зумовлює міжкваркові взаємодії. Частинки міжкваркового поля називаються глюонами. Експериментально глюони поки що не виявлені. Нарешті, мають бути кванти поля слабких взаємодій — векторні базони. Вони також поки що не виявлені.
Отже, картина будови матерії на самому глибокому рівні виявилася досить складною. Побудова кількісної теорії міжкваркових сил ще не завершена. Можливо, згодом будуть виявлені ще масивніші кварки і лептони.
Розв’язуємо разом
1. Чому нейтрони є найкращими снарядами для руйнування ядра атома, ніж протони, електрони, а-частинки?
Розв’язання
Нейтрон завдяки своїй нейтральності з будь-якою енергією (від часток до кількох мільонів електрон-вольт), вільно проникає в будь-яке ядро, включаючи і важкі. Але в кожному конкретному випадку частинки-снаряди повинні мати відповідну енергію.
2. Скільки відбувається а- і β-розпадів під час радіоактивного розпаду
Розв'язання
Радіоактивний розпад урану можна записати так:
Нагадаємо, що а-частинка — це  а β-частинка — це
а β-частинка — це 
Застосовуючи закон збереження зарядових чисел, можна записати
92 = 82 + 2x- 1у.
Застосувавши закон збереження масових чисел, отримаємо
238 = 198 + 4х.
Розв’язуючи отримані рівняння як систему, маємо х = 10 і у= 10, тобто відбувається десять a-розпадів і десять β-розпадів.
3. При зіткненні а-частинки з ядром бора 10 5В відбулась ядерна реакція, внаслідок якої утворилося два нових ядра. Одним з цих ядер було ядро атома Гідрогену 1 1Н . Визначте порядковий номер і масове число другого ядра, дайте символічний запис ядерної реакції і визначте її енергетичний ефект.
Розв’язання
Позначимо невідоме ядро символом 
Знаючи, що а-частинка — це ядро Гелію  запис реакції матиме вигляд
запис реакції матиме вигляд 
«Застосувавши закон збереження числа нуклонів, отримаємо рівняння 4+10=1 + А, звідки А = 13.
Застосувавши закон збереження заряду, маємо 2 + 5 = 1 + Z, звідки Z = 6.
Отже, невідоме ядро є ядром атома ізотопу Карбону 136C .
Тепер рівняння можна записати в кінцевому вигляді
Енергетичнии ефект ядерної реакції визначається за формулою
Використовуючи табличні значення маси атомів, отримаємо
Q = 931[(4,00260 +10,01294) - (1,00783+13,00335)] МеВ = 4,06 МеВ .
Q = 4,06 МеВ.
4. Визначте добові витрати урану 238 92U атомною електростанцією потужністю 7 МВт, якщо ККД електростанції 20 %. При кожному розпаді виділяється енергія 200 МеВ.
Розв’язання
Якщо при кожному розпаді виділяється енергія Е0, то при розпаді за добу, припустимо N атомів (ядер), виділиться енергія Е = NE0. Нехай N атомів відповідає масі урану т кг, тоді 
де Na — число Авогадро; μ — молярна маса урану.
Енергія, яка виділяється за добу, розраховується за формулою:
а повна енергія: Е = ηE1 = Pt, де Р — потужність електростанції, t = 1 доба = 86 400 с.
Тоді  .
.
Підставивши значення відомих фізичних величин, отримаємо
m = 36, 8 10-3 кг.
Домашнє завдання: опрацювати тему , написати та вивчити конспект.
Дата уроку : 04.05.20
Тема уроку: Ланцюгова ядерна реакція поділу ядер Урану. Термоядерні реакції.
1.
Ядерну реакцію поділу атомних ядер уперше спостерігали у 1939 р. німецькі вчені О. Ган і Ф. Штрасман. Вони встановили, що під час бомбардування ядер атомів Урану нейтронами вони діляться на дві приблизно однакові частинки (мал. 8.5).
Внаслідок кожного такого поділу вивільняється 2—3 нейтрони і близько 200 МеВ енергії. Ф. Жоліо-Кюрі висловив думку, що під впливом потоку вивільнених нейтронів ядерна реакція поділу ядер атомів Урану може розвиватися як ланцюгова.
Ядерною ланцюговою реакцією називають реакцію, в якій частинки (нейтрони), що спричиняють її, утворюються як продукти цієї реакції.
Щоб ланцюгова реакція розвивалася, потрібно підтримувати незмінним потік нейтронів і створити умови для їх проникнення в ядра атомів Урану. З цією метою треба достатню масу Урану вміщувати в обмеженому просторі, створювати так звані критичні умови. Тоді нейтрони потраплятимуть в ядра, викликаючи подальший їх поділ. Мінімальну масу, за якої ланцюгова реакція відбувається самочинно, називають критичною. Для чистого УрануU, що має форму кулі, критична маса приблизно дорівнює 50 кг . Радіус такої кулі дорівнює приблизно 9см.
Здійснення ланцюгової реакції поділу ядер атомів Урану — досить складний процес. Адже повільні нейтрони, що вивільняються в процесі ядерної реакції, можуть викликати поділ лише ядер 23592U; для поділу ядер 23892U потрібні швидкі нейтрони з енергією понад 1 МеВ. Оскільки природний Уран складається з двох нуклонів — 99,3 % Урану-238 і лише 0,7 % Урану-235, то для підтримання ланцюгової ядерної реакції необхідно задовольнити принаймні дві умови: досягти критичної маси і забезпечити достатнє число вивільнених нейтронів для підтримання реакції, яке б не зменшувалося з часом.
Повільні нейтрони не викликають поділу ядра 23892U. Проте їх захоплення цим нуклідом веде до цікавих наслідків — утворення трансуранових елементів. Трансуранові елементи — це хімічні елементи, розміщені в таблиці Менделєєва за Ураном (Z > 92)
Спочатку виникає короткоживучий радіоактивний нуклід 23992U, період піврозпаду якого Т = 23 хв (мал. 8.6), який внаслідок бета-розпаду перетворюється на новий елемент — Нептуній:
У свою чергу, нестійкий нуклід нептунію перетворюється на відносно стабільний Плутоній
Т = 24 000 років:
Ядерну реакцію одержання Плутонію нині широко використовують у сучасних ядерних реакторах - розмножувачах.
Від повного поділу всіх ядер 1г Урану виділяється 2,3·10 кВт·год енергії, яка еквівалентна енергії, що утворюється від спалювання 3т вугілля, або 2,5т нафти.
кВт·год енергії, яка еквівалентна енергії, що утворюється від спалювання 3т вугілля, або 2,5т нафти.
Пристрій, в якому підтримується керована реакція поділу ядер, називається ядерним (атомним) реактором.
Ядерний реактор складається з: активної зони, де відбувається ядерна реакція, поглиначів нейтронів, захисного кожуха, парогенератора, турбіни та електричного генератора (мал. 8.7).
Принцип його дії полягає у використанні вивільненої внаслідок ядерної реакції енергії для здобуття електричної напруги.
В активну зону завантажують ядерне паливо — збагачений Уран у вигляді тепловидільних елементів (ТВЕЛів), які утворюють правильну ґратку, і речовину, що гальмує нейтрони (графіт або так звану важку воду), оскільки ядра нукліда урану-235 краще захоплюють повільні нейтрони.
В активну зону завантажують ядерне паливо — збагачений Уран у вигляді тепловидільних елементів (ТВЕЛів), які утворюють правильну ґратку, і речовину, що гальмує нейтрони (графіт або так звану важку воду), оскільки ядра нукліда урану-235 краще захоплюють повільні нейтрони.
Щоб ланцюгова реакція була керованою, необхідно регулювати число нейтронів в активній зоні. З цією метою до неї вводять регулювальні стрижні з матеріалу, який добре вбирає нейтрони (Кадмій, Бор). Зміною глибини їх введення регулюють потік нейтронів, а отже, керують перебігом ланцюгової реакції.
Енергія, що виділяється в результаті поділу ядер атомів Урану, за допомогою теплоносія передається парогенератору.
Вироблена ним водяна пара спрямовується на лопатки парової турбіни, сполученої з генератором, який виробляє електроенергію. Так після кількох перетворень енергія, що вивільняється внаслідок поділу атомних ядер, стає електричною. Електромережами вона потрапляє до споживачів.
Потужність ядерного реактора в 1 МВт відповідає ланцюговій реакції, за якої відбувається
3 ∙ 1016 актів поділу ядер Урану за 1 с
Основні елементи ядерного реактора:
· ядерне паливо (U, Pu, U); сповільнювач нейтронів (важка або звичайна вода, графіт);
· теплоносій для виведення енергії, що утворюється під час роботи реактора (вода, рідкий натрій);
· пристрій для регулювання швидкості реакції (стержні, які вводять у робочий простір реактора; вони містять Кадмій чи Бор – речовини, які добре поглинають нейтрони).
Зовні реактор оточують захисною оболонкою, що затримує γ-проміння і нейтрони. Її роблять з бетону із залізним заповнювачем. Існує декілька видів ядерних реакторів:
- Реактори на швидких нейтронах (реактори-розмножувачі).
- Реактор на повільних нейтронах
Перша ядерна реакція була здійснена у США у грудні 1942 році колективом вчених під керівництвом Енріко Фермі.
У Радянському Союзі перший ядерний реактор було запущено 25 грудня 1946 року колективом фізиків під керівництвом І. В. Курчатова.
Ядерні реактори є основою атомних електростанцій (АЕС). Нині у світі налічується понад 1000 ядерних енергетичних установок. Атомна енергетика вважається економічно найвигіднішою і високотехнологічною. Вона використовує останні досягнення науки, сучасні автоматизовані системи керування технологічним процесом на основі ЕОМ, потребує високої кваліфікації працівників. Експлуатація АЕС потребує запровадження широкого спектра засобів контролю і радіаційної безпеки, оскільки в разі нехтування ними наслідки можуть бути катастрофічними. 26 квітня 1986 р. внаслідок грубого порушення технологічного циклу роботи ядерного реактора на Чорнобильській АЕС сталася аварія. Загинули люди, наслідки цієї трагедії відчуваються досі.
Загальновідомо, що при розподілі важких ядер атомів під час ядерних реакцій виділяється велика кількість енергії. Проте вдалося встановити, що при злитті легких ядер виділяється ще більшу кількість енергії. Такі реакції назвали термоядерними.
Загальновідомо, що при розподілі важких ядер атомів під час ядерних реакцій виділяється велика кількість енергії. Проте вдалося встановити, що при злитті легких ядер виділяється ще більшу кількість енергії. Такі реакції назвали термоядерними.
Перша термоядерна реакція була здійснена в 1932 році на швидких протонах
У природних умовах термоядерні реакції синтезу відбуваються в надрах зірок і є основним джерелом їхньої енергії. Для Сонця основною реакцією є перетворення чотирьох протонів на ядро атома Гелію, що супроводжується виділенням енергії понад 26 МеВ за один цикл. У земних умовах досягти таких температур можна лише за допомогою ядерного вибуху (на цьому ґрунтується принцип дії водневої бомби) або в потужному імпульсі лазерного випромінювання (керована термоядерна реакція синтезу).
Природа термоядерних реакцій
Термоядерні реакції — це реакції злиття легких ядер, що протікають при високих температурах з виділенням великої кількості енергії. Синтез гелію з водню протікає при t = 108 ˚ К. При синтезі одного грама гелію виділяється 4,2 ∙1011 Дж. Ця енергія еквівалентна енергії, що виділяється при повному розподілі4 грамів урану або при спалюванні 10 тонн дизпалива. Термоядерні реакції можна зустріти в зірках, де температура і тиск речовини створюють придатні умови для здійснення злиттів.
Термоядерні реакції — це реакції злиття легких ядер, що протікають при високих температурах з виділенням великої кількості енергії. Синтез гелію з водню протікає при t = 108 ˚ К. При синтезі одного грама гелію виділяється 4,2 ∙1011 Дж. Ця енергія еквівалентна енергії, що виділяється при повному розподілі
У термоядерної реакції синтезу гелію беруть участь ізотопи водню: тритій і дейтерій:
При злитті дейтерію і тритію в ядро гелію виділяється нейтрон і енергія E = 17,6 МеВ.
Умови протікання термоядерних реакцій
Для протікання термоядерних реакцій потрібні певні умови. Потрібен зблизити ядра зазначених ізотопів. Ядра атомів мають позитивний заряд, і, отже, при їх зближенні діють кулонівських сили, розштовхують ці заряди.
Відповідно, для злиття ядер необхідно подолати відразливі сили. Це можливо лише у випадку, якщо самі ядра володіють дуже великою енергією, в першу чергу, кінетичної енергією руху, тобто тоді, коли їх швидкість досить велика.
Ядра ізотопів можуть володіти такою швидкістю тільки при дуже високій температурі. Необхідно додати часткам швидкість достатню, щоб вони могли наблизитися один до одного на відстань ≈ 10 -14 м . На такій відстані вже починають діяти ядерні сили тяжіння.
Подібної температури можна домогтися лише при вибуху атомної бомби. Тобто, щоб справити термоядерну реакцію, треба провести спочатку ядерну реакцію, і тоді температури буде достатньо для зближення ядер ізотопів водню і здійснення термоядерної реакції. Такий процес був реалізований у водневій бомбі — найпотужнішої з винайдених людиною.
Керовані термоядерні реакції
Однак на сьогоднішній день некерована термоядерна реакція — це вже не актуально. Необхідно освоїти керовану термоядерну реакцію, щоб перетворювати одержувану енергію в електричну. Але є проблема. При досягненні температури, достатньої для здійснення реакції злиття легких ядер, речовина вже перестає бути не тільки твердим, рідким або газоподібним, воно стає плазмою.
Тобто, будь-який реактор моментально випарується при таких температурах. Тут потрібно зовсім інший підхід. На сьогоднішній день вдається утримувати плазму на обмеженій території за допомогою надпотужних електричних магнітів. Але повноцінно використовувати одержувану в результаті термоядерної реакції енергію поки не вдається.
Це питання майбутнього. Однак це питання необхідно вирішувати, тому що запаси водню, тобто палива, у Всесвіті практично невичерпні, а земні запаси палива, навпаки, підходять до кінця. Керована термоядерна реакція може раз і назавжди позбавити людство від енергетичних проблем.
Домашнє завдання : написати та вивчити конспект.
Дата уроку : 29.04.20
Тема уроку: Експериментальна робота № 9. Дослідження треків заряджених частинок за фотографіями.
Домашнє завдання : виконати експериментальну роботу, всі дані є у відео, виконуємо тільки1 варіан, без додаткового завдання.
Дата уроку : 28.04.20
Тема уроку: Отримання та застосування радіонуклідів. Методи реєстрації іонізуючого випромінювання.
Радіаційний вплив випромінювання на речовину.Поглинання енергії
Поглинена доза випромінювання D — це фізична величина,яка чисельно дорівнює енергії випромінювання,поглиненій одиницею маси речовини
D = W/m, де W - енергія іонізуючого випромінювання, передана речовині, m – маса цієї речовини На практиці [ D] = рад.
Назва походить від англійської абревіатури ( rad – radiation absorbed dose). 100 рад = 1Гр (грей)
D = W/m, де W - енергія іонізуючого випромінювання, передана речовині, m – маса цієї речовини На практиці [ D] = рад.
Назва походить від англійської абревіатури ( rad – radiation absorbed dose). 100 рад = 1Гр (грей)
Поглинена доза накопичується з часом
1Гр – це поглинена доза випромінювання , за якої речовині масою 1кг передається енергія іонізуючого випромінювання, що дорівнює 1 Дж Відношення поглинутої дози до часу опромінення називають потужністю РD поглиненої] дози випромінювання: РD = D/t, де D - поглинена доза випромінювання, t – час опромінення
Іонізація
Експозиційна доза випромінювання визначається кількістю заряду (байдуже з яким знаком), що виник під дією випромінювання, в 1 кг повітря.
[1 ] = Кл/кг
1 Кл/кг – це експозиційна доза випромінювання, за якої сумарний заряд усіх іонів одного знака, що утворилися в 1 кг повітря, дорівнює 1 Кл.
На практиці [D] = Р (рентген).
1Р = 2,58 · 10 - 4 Кл/кг
[1 ] = Кл/кг
1 Кл/кг – це експозиційна доза випромінювання, за якої сумарний заряд усіх іонів одного знака, що утворилися в 1 кг повітря, дорівнює 1 Кл.
На практиці [D] = Р (рентген).
1Р = 2,58 · 10 - 4 Кл/кг
Еквівалентна доза іонізуючого випромінювання ( ) враховує різну радіаційну небезпеку різних іонізуючих випромінювань. Вона дорівнює поглиненій дозі, помноженій на коефіцієнт якості k, який є неоднаковим для різних випромінювань= k · D
[ 1] = Зв (зіверт);
[1 ] = бер
Безпечні для людини дози опромінення подають у мілізівертах (мЗв). Доза опромінення в 1 Зв викликає небезпечні зміни крові, а після опромінення дозою в
4-5Зв можлива смерть
[1 ] = бер
Безпечні для людини дози опромінення подають у мілізівертах (мЗв). Доза опромінення в 1 Зв викликає небезпечні зміни крові, а після опромінення дозою в
4-5Зв можлива смерть
Методи реєстрації радіоактивних випромінювань
Фізична суть роботи приборів для реєстрації радіоактивних випромінювань: макроскопічна система перебуває в нестійкому стані. Радіоактивне випромінювання призводить до того, що система переходить до стійкого стану. Під час переходу фіксується частинка. В основі методів реєстрування та дослідження властивостей радіоактивних випромінювань – іонізуючі та фотохімічні дії частинок та випромінювання, відхилення заряджених частинок у магнітному полі.
№ Прилади Принцип дії
1 Камера Вільсона Конденсація переохолодженої пари
2 Система Вільсона – Скобельцина Камера Вільсона в магнітному полі, На заряджені частинки діє
3 Бульбашкова камера
(Д. Глейзер) Закипання перегрітої рідини
4 Лічильник Гейгера Самостійний газовий розряд, який виникає за ударної іонізації
5 Фотоемульсії на пластинках
(Беккерель, Жданов) Фотохімічна реакція в AgBr
6 Сцинтиляційні лічильники Сцинтиляції на екрані, покритому спеціальною речовиною
1 Камера Вільсона Конденсація переохолодженої пари
2 Система Вільсона – Скобельцина Камера Вільсона в магнітному полі, На заряджені частинки діє
3 Бульбашкова камера
(Д. Глейзер) Закипання перегрітої рідини
4 Лічильник Гейгера Самостійний газовий розряд, який виникає за ударної іонізації
5 Фотоемульсії на пластинках
(Беккерель, Жданов) Фотохімічна реакція в AgBr
6 Сцинтиляційні лічильники Сцинтиляції на екрані, покритому спеціальною речовиною
Основні радіологічні величини та одиниці
Величина .Найменування та позначення..Одиниці вимірювання Зв'язок між одиницями
Позасистемні СІ
Активність нукліду, А Кюрі (Ки) Беккерель (Бк) 1 Ки= 3,7 ·10¹⁰Бк
1 Бк = 1 розп/с
1 Бк=2,7 · 10⁻¹¹( Ки)
Експозиційна доза Рентген (Р) Кулон/кг
(Кл/кг) 1 Р= 2,58 · 10⁻⁴ Кл/кг
Позасистемні СІ
Активність нукліду, А Кюрі (Ки) Беккерель (Бк) 1 Ки= 3,7 ·10¹⁰Бк
1 Бк = 1 розп/с
1 Бк=2,7 · 10⁻¹¹( Ки)
Експозиційна доза Рентген (Р) Кулон/кг
(Кл/кг) 1 Р= 2,58 · 10⁻⁴ Кл/кг
1Кл/кг = 3,88 ·10³ Р
Поглинена доза Рад (рад) Грей (Гр) 1 рад = 10⁻²Гр
1 Гр = 1 Дж/кг
Еквівалентна доза Бер (бер) Зіверт (Зв) 1 бер = 10⁻² Зв
1 Зв = 100 бер
Інтегральна доза випромінювання Рад-грам (рад·г) Грей-кг (Гр•кг) 1 рад · г = 10⁻⁵Гр•кг
1 Гр·кг= 10⁵ рад· г
Поглинена доза Рад (рад) Грей (Гр) 1 рад = 10⁻²Гр
1 Гр = 1 Дж/кг
Еквівалентна доза Бер (бер) Зіверт (Зв) 1 бер = 10⁻² Зв
1 Зв = 100 бер
Інтегральна доза випромінювання Рад-грам (рад·г) Грей-кг (Гр•кг) 1 рад · г = 10⁻⁵Гр•кг
1 Гр·кг= 10⁵ рад· г
Вплив радіації на організм людини
Іонізуюче випромінювання:
Рентгенівське випромінювання, гама-випромінювання,
Альфа-частинки, електрони, протони, нейтрони.
Рентгенівське випромінювання, гама-випромінювання,
Альфа-частинки, електрони, протони, нейтрони.
Найбільш поширені хвороби в результаті опромінення:
• Ракові пухлини;
• Лейкемія;
• Променева хвороба.
• Ракові пухлини;
• Лейкемія;
• Променева хвороба.
Залежно від рівня біологічної організації радіобіологи виділяють такі
види біологічного ураження іонізуючим випромінюванням:
• молекулярний (ураження молекул РНК, ДНК, негативний влив на процеси обміну);
• субклітинний (ураження біомембран та складових клітини);
• клітинний (уповільнення процесів ділення клітин, часткове перетворення їх у злоякісні);
• тканинний (ураження чутливих тканин та органів);
• організмовий (зменшення строку життя, швидка загибель);
• популяційний (зміна генетичних характеристик окремих організмів).
Захист від радіації:
• Віддалення від джерела випромінювання на значні відстані;
• Захисний одяг;
• Перешкоди з поглинальних матеріалів;
• Особливий режим харчування та використання води;
• Медикаментозне лікування.
види біологічного ураження іонізуючим випромінюванням:
• молекулярний (ураження молекул РНК, ДНК, негативний влив на процеси обміну);
• субклітинний (ураження біомембран та складових клітини);
• клітинний (уповільнення процесів ділення клітин, часткове перетворення їх у злоякісні);
• тканинний (ураження чутливих тканин та органів);
• організмовий (зменшення строку життя, швидка загибель);
• популяційний (зміна генетичних характеристик окремих організмів).
Захист від радіації:
• Віддалення від джерела випромінювання на значні відстані;
• Захисний одяг;
• Перешкоди з поглинальних матеріалів;
• Особливий режим харчування та використання води;
• Медикаментозне лікування.
Джерела опромінення:
• Природний радіаційний фон;
• Продукти ядерних вибухів;
• Робота установ, які використовують радіоактивні препарати;
• Медична діагностика;
• Будівельні матеріали;
• Телебачення, мобільний зв'язок та комп'ютери;
• Атомні електростанції.
Домашнє завдання : Написати та вивчити конспект з даної теми.• Природний радіаційний фон;
• Продукти ядерних вибухів;
• Робота установ, які використовують радіоактивні препарати;
• Медична діагностика;
• Будівельні матеріали;
• Телебачення, мобільний зв'язок та комп'ютери;
• Атомні електростанції.
Дата уроку : 27.04.20
Тема уроку: Експериментальна робота № 8. Моделювання радіоактивного розпаду.
Мета роботи: перевірити математичну залежність, що описує закон радіоактивного розпаду і побудувати графік розпаду.
Прилади і матеріали: монети, дві пластикові банки, рознос.
Теоретичні відомості.
Крім сталої розпаду радіоактивний розпад можна характеризувати періодом піврозпаду Т.
Період піврозпаду – це час, протягом якого число наявних радіоактивних ядер зменшується вдвічі.
Якщо час t1=T, то число ядер, що залишилися, дорівнює  ; через два періоди t2=2T :
; через два періоди t2=2T : 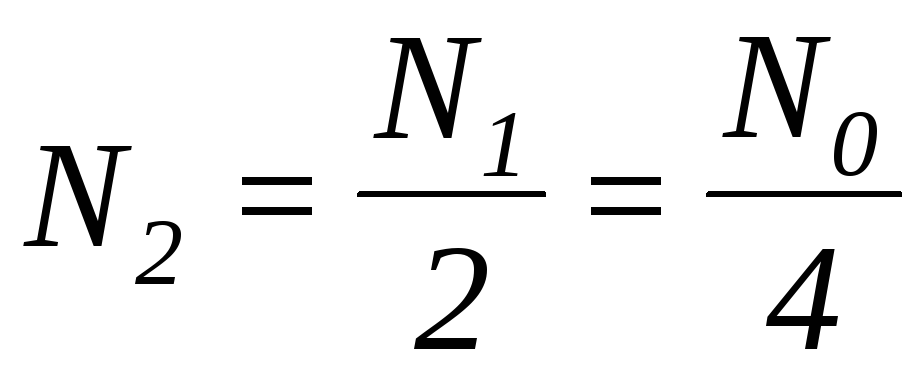 ; через три періоди t3=3T :
; через три періоди t3=3T : 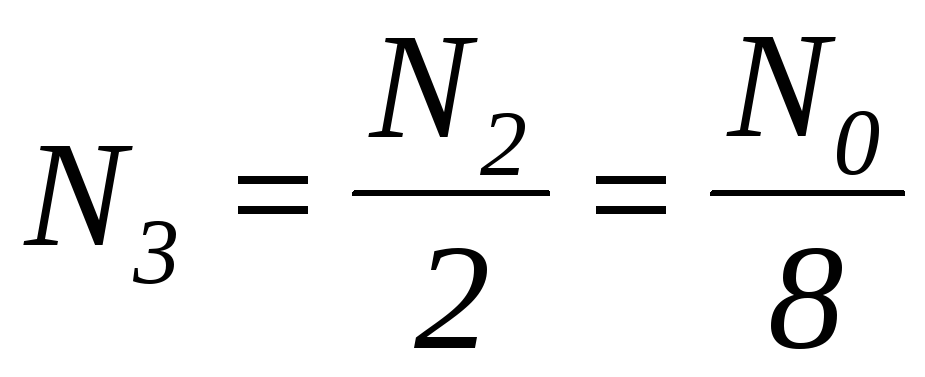 і т.д. Перепишемо вирази для N1, N2, N3 наступним чином:
і т.д. Перепишемо вирази для N1, N2, N3 наступним чином: 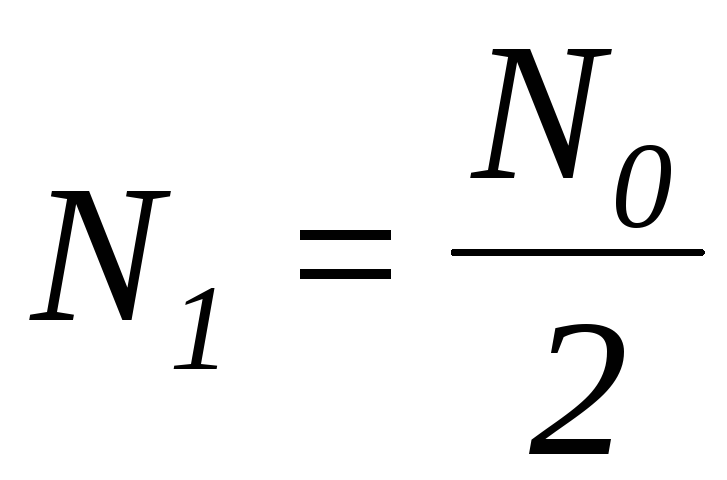 ;
; 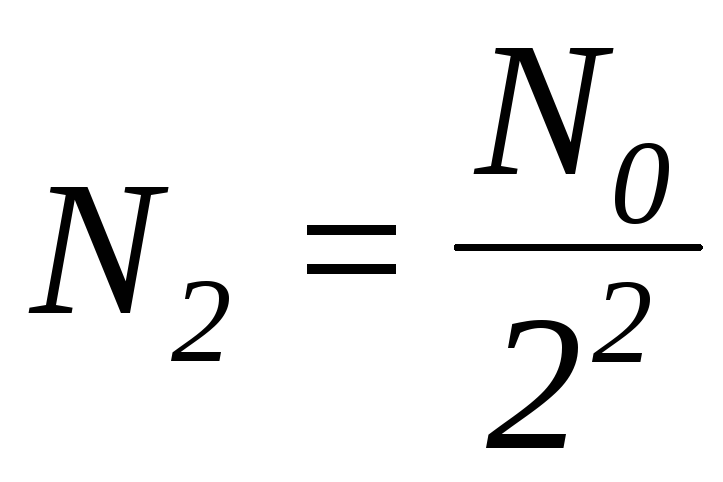 ;
; 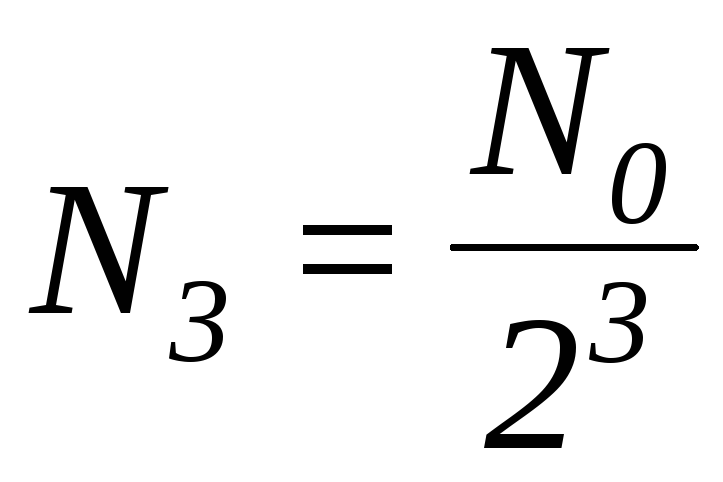 .
.
Легко бачити закономірність, яку можна подати в загальному виді: 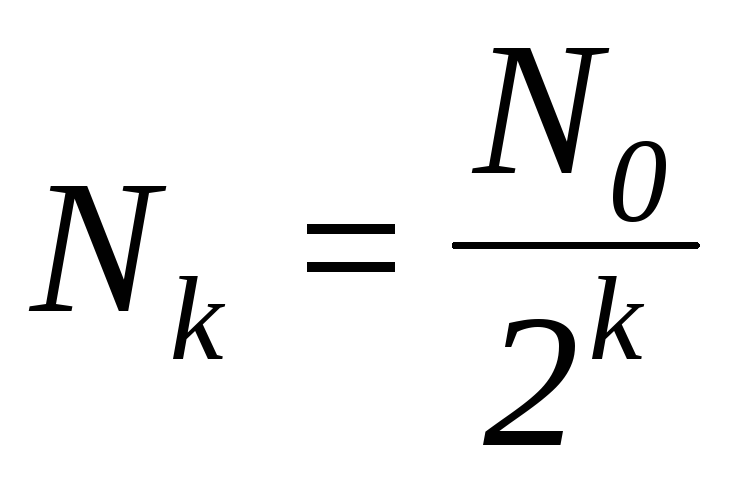 , де
, де 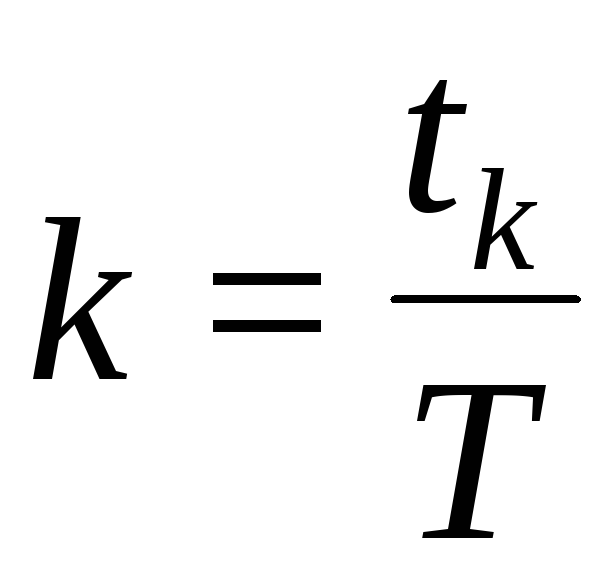 . Для довільного моменту часу t:
. Для довільного моменту часу t:
 або або |
(3)
|
(3)- це ще одна форма запису закону радіоактивного розпаду.
Вираз (3) можна одержати також і з рівняння (2).
Якщо 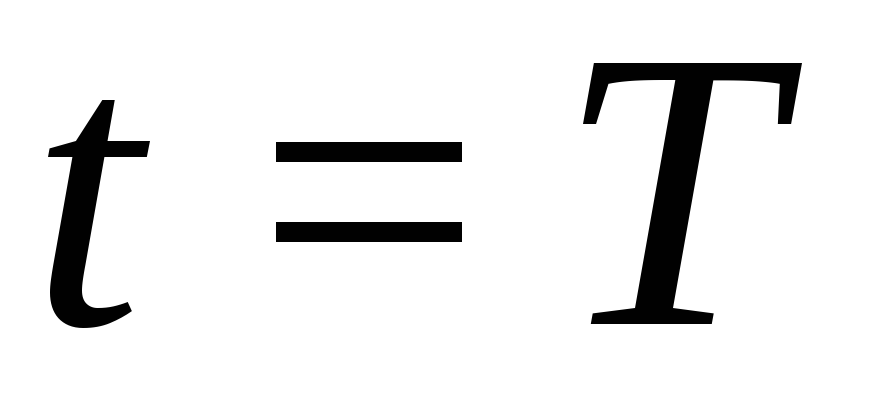 , то
, то 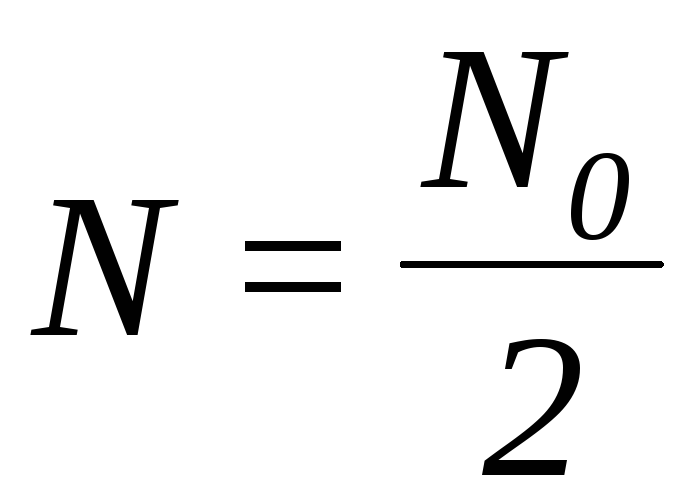 :
:  ; скоротивши на N0, матимемо:
; скоротивши на N0, матимемо: 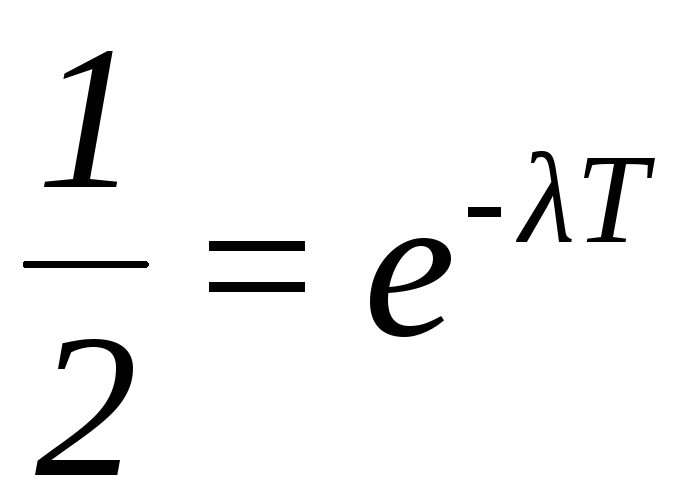 , або
, або 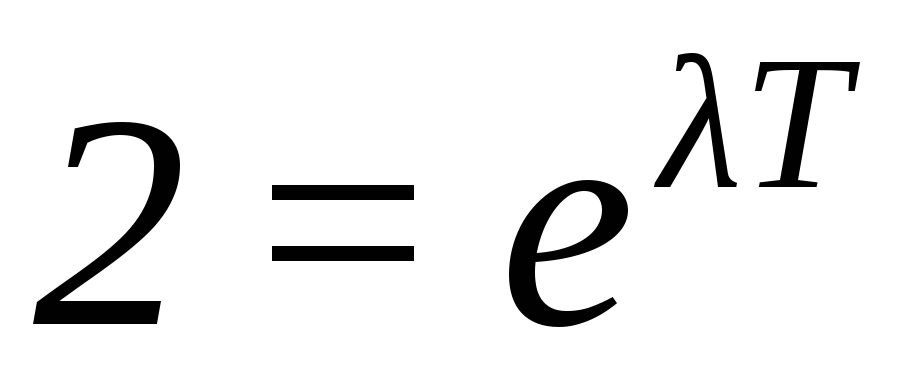 .
.
Прологарифмуємо цей вираз: 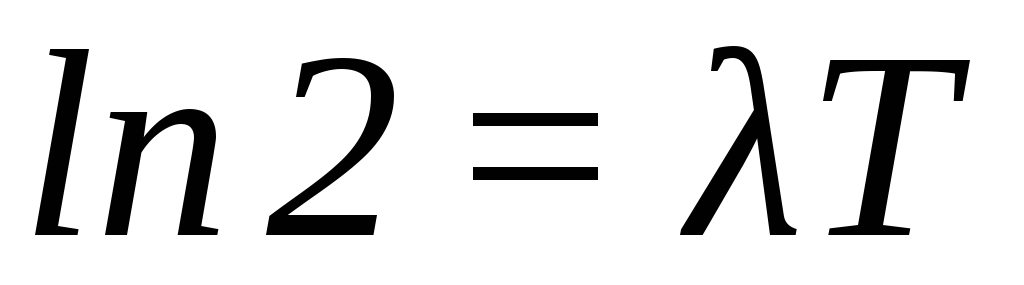 , звідки:
, звідки:
(4)
|
Вираз (4) дає зв’язок між сталою радіоактивного розпаду і періодом піврозпаду. Підставимо (4) в (2): 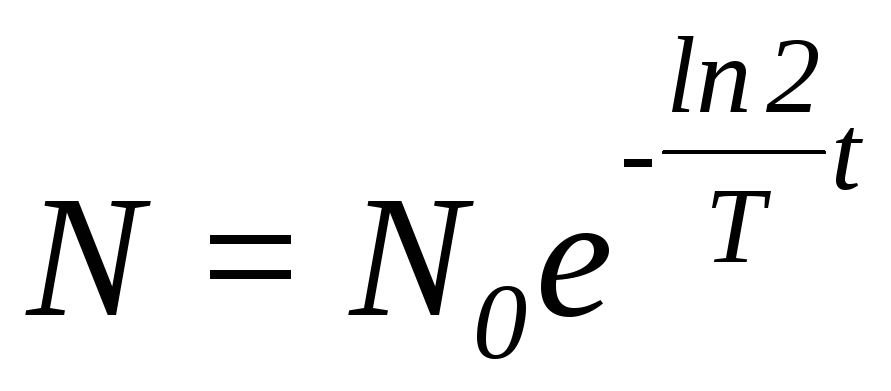 ; після перетворень одержимо:
; після перетворень одержимо: 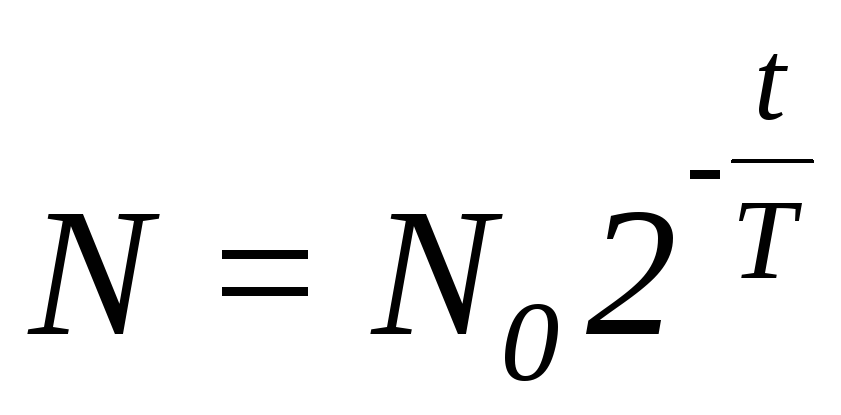 , що співпадає з виразом (3).
, що співпадає з виразом (3).
Число ядер, що розпались за час t, дорівнює:
(5)
|
Закон радіоактивного розпаду передбачає число ядер, які не розпались за час t; але він не вказує, які саме ядра розпадуться за цей час. Цей закон є статистичним законом; точно він виконується лише у випадку величезної кількості ядер.
Імовірність розпаду кожного з радіоактивних ядер за час T дорівнює 1/2. Процес радіоактивного розпаду можна моделювати підкиданням монет, при якому з імовірністю 1/2 випадає герб чи цифра ("орел" чи "решка"). Нехай, якщо випаде "орел", то ядро вціліло, а якщо "решка" - то розпалось. Кожне кидання монет відповідає для ядра протіканню проміжку часу, що дорівнює періоду піврозпаду.
Хід роботи.
1. Відрахуйте 128 монет (N0=128), перемішайте їх у банці і висипте на рознос.
2. Підрахуйте число монет, що "не розпались" ("орел"), і складіть їх знову в банку. В іншу банку складіть монети, що "розпалися".
3. Перемішайте монети, що "не розпались", і висипте на рознос. Повторіть п.2.
4. Пункт 3 повторюйте до тих пір, поки всі монети "розпадуться".
5. Кількість монет, що "не розпалися" при черговому киданні , і кількість монет, що "розпались" за n кидань, занесіть в таблицю 1.
6. Повторіть серію кидань ще двічі, щоразу починаючи з N0=128. Результати дослідів занесіть в таблиці 2 і 3, що аналогічні табл.1.
7. Побудуйте графік залежності N(n). Всі серії зобразіть на одному рисунку, використавши різнокольорові ручки. На цьому ж рисунку зобразіть теоретичну залежність 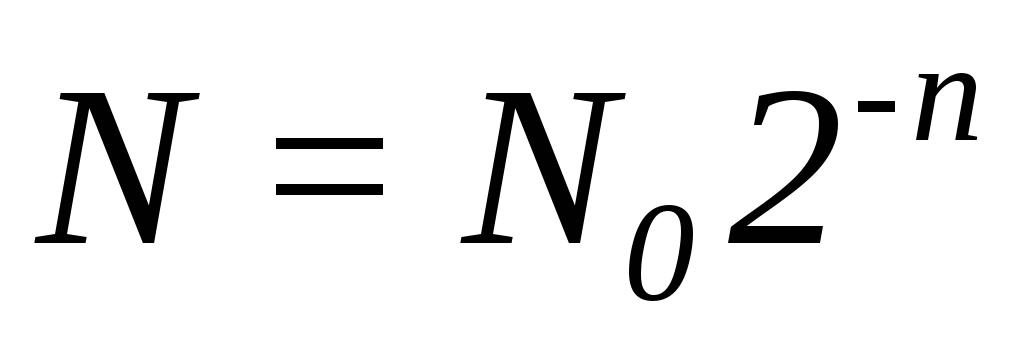 .
.
8. Зробіть висновок.
Контрольні запитання
1. Який склад атома і атомного ядра?
2. Що являють собою α , β - частинки та γ - промені?
3. Які способи реєстрації іонізуючих випромінювань ви знаєте?
4. Який фізичний зміст сталої розпаду.?
5. Що називають періодом піврозпаду Т?
6. Який зв’язок між сталою розпаду. і Т?
5. Який елемент слід вважати більш радіоактивним: з періодом піврозпаду 1 доба чи 1 година? Чому?
Табл. 1
Кількість кидань n
|
0
|
1
|
2
|
3
|
4
|
5
|
6
|
7
|
8
|
9
|
10
|
Кількість монет, що
"не розпались", N
|
128
| ||||||||||
Кількість монет, що
"розпались", N'
|
0
|
Дата уроку : 22.04.20
Тема уроку:Розв"язування задач.
1. Визначте період піврозпаду радіоактивного елемента, якщо через інтервал часу 1,2 с число атомів, що розпалися, становить 87,5 % їх початкової кількості. Відповідь подайте в секундах.
Розв'язання
За інтервал часу ∆t1 = Т розпалося 50 % ядер; залишилося 50%.
За інтервал часу ∆t2 = Т розпалась половина ядер від 50 % решти (тобто ще 25 %), усього розпалося 75 % ядер; залишилося 25 %.
За інтервал часу ∆t3 = Т розпалась половина ядер від 25 % решти (тобто ще 12,5 %), усього розпалось:
75 + 12,5 = 87,5(%).
Таким чином, за інтервал часу ∆t = ∆t1 + ∆t2 + ∆t2 = 3T розпалося 87,5 % ядер від початкової кількості.
За умовою задачі ∆t = 1,2 с, тобто 3Т = 1,2 с  Т =
Т =  = 0,4 (с).
= 0,4 (с).
Відповідь: 0,4 с.
Під час розв'язування задач па визначення періоду напіврозпаду слід розуміти, що період піврозпаду Т — це час, за який розпадається половина ядер наданого зразка.
• Якщо ∆t = 2Т, то розпадеться вже  ядер (половина + половина половини), тобто 75 %, а залишиться 25 % від початкової кількості ядер тощо.
ядер (половина + половина половини), тобто 75 %, а залишиться 25 % від початкової кількості ядер тощо.
Дата уроку :21.04.20
Тема уроку: Радіоактивність . Основний закон радіоактивного розпаду.
Ви вже знаєте, що радіоактивність — це явище, яке свідчить про складну будову атомного ядра. Рентгенівські промені,вперше були одержані внаслідок зіткнення швидких електронів з антикатодом розрядної трубки. А. Беккерель довго досліджував споріднене явище — післясвічення речовин, які перед тим були опромінені сонячним світлом. До таких речовин, зокрема, належать солі урану, з якими він експериментував.
А чи не виникають після опромінення солей урану разом з видимим світлом і рентгенівські промені?
А. Беккерель загорнув фотопластинку в цупкий чорний папір, зверху поклав шматочки уранової солі і виставив це на яскраве сонячне світло. Під час проявлення пластинка почорніла на тих місцях, де лежала сіль. Отже, уран випускає промені, які, подібно до рентгенівських, пронизують непрозорі тіла і діють на фотопластинку. Вчений вважав, що таке випромінювання виникає під впливом сонячного світла. Однак, в лютому 1896 р. Беккерелюне вдалося зробити черговий дослід і він поклав пластинку, на якій лежав мідний хрест, вкритий сіллю урану, в ящик стола. Проявивши на всяк випадок пластинку через два дні, він виявив на ній почорніння у вигляді виразної тіні хреста. Це означало, що солі урану спонтанно, без впливу зовнішніх чинників утворюють якесь проміння.
Незабаром Беккерель виявив, що промені уранової солі йонізують повітря так само, як і рентгенівські, і тому розряджають електроскоп. Випробовуючи різні хімічні сполуки урану, він установив дуже важливий факт: інтенсивність випромінювання визначається лише кількістю урану в препараті і зовсім не залежить від того, до яких сполук він входить. Отже, це властивість не сполук, а хімічного елемента урану, його атомів.
У 1898 р. у Франції Марія Склодовська-Кюрі та інші вчені виявили випромінювання торію. Особливо плідною у пошуках нових елементів виявилася праця подружжя Марії і П’єра Кюрі. Систематичне дослідження руд, що містять уран і торій, дало їм можливість виділити новий, ще невідомий хімічний елемент полоній, названий так на честь батьківщини Марії Склодовської-Кюрі — Польщі.
Нарешті, було відкрито ще один елемент, якому властиве дуже інтенсивне випромінювання. Його назвали радієм (тобто променистим). Саме ж явище спонтанного випромінювання подружжя Кюрі назвало радіоактивністю.
Після відкриття радіоактивних елементів почалося дослідження фізичної природи їхнього проміння. Крім Беккереля й подружжя Кюрі, над цим питанням почав працювати Резерфорд.
Класичний дослід, який допоміг виявити склад радіоактивного випромінювання, полягав у такому. Радіоактивний препарат вміщували на дно вузького каналу в шматку свинцю. Проти каналу розташовували фотопластинку. На проміння, яке виходило з каналу, діяли сильним магнітним полем (мал. 207), перпендикулярним до нього. Всю установку розміщали у вакуумі.
Якщо не було магнітного поля, то на проявленій пластинці було виявлено одну тільки темну пляму, точно проти каналу. У магнітному ж полі

Мал. 207
пучок розпадався на три пучки. Дві складові первинного потоку відхилялись у протилежні боки. Це переконливо вказувало на те, що вони мають електричні заряди протилежних знаків. При цьому негативну складову проміння магнітне поле відхиляло значно більше, ніж позитивну. Третю складову магнітне поле не відхиляло. Позитивно заряджена складова випромінювання отримала назву альфа-випромінювання, негативно заряджена — бета-випромінювання, а нейтральна — гамма-випромінювання (а-промені , (β-промені, γ-промені).
Ці три види випромінювання дуже різняться між собою за проникною здатністю, тобто за тим, наскільки інтенсивно їх поглинають різні речовини. Найменшу проникну здатність мають а-промені. Шар паперу товщиною близько 0,1 мм для них вже непрозорі. Якщо отвір у свинцевій пластинці прикрити аркушиком паперу, то на фотопластинці не буде плями, що відповідає а-променям.
Значно менше поглинаються речовиною β-промені. Алюмінієва пластинка затримує їх цілком лише тоді, коли її товщина досягає кількох міліметрів. Найбільшу проникну здатність мають у-промені. Інтенсивність їх поглинання збільшується зі зростанням атомного номера речовини-поглинача. Але й шар свинцю товщиною сантиметр — не перешкода для цих променів. Від проходження крізь таку пластинку їхня інтенсивність зменшується лише в два рази. Це пов’язано з тим, що фізична природа а-, (- і γ-променів різна.
А. Ейнштейн і Ф. Содді встановили, що атомам деяких елементів властивий спонтанний розпад, який супроводжується випромінюванням величезної кількості енергії порівняно з енергією, яка вивільняється в процесі звичайних молекулярних видозмін.
Після того як було відкрито атомне ядро, відразу стало зрозуміло, що саме воно зазнає змін під час радіоактивних перетворень. Адже а-частинок взагалі немає в електронній оболонці, а зменшення кількості електронів оболонки на одиницю перетворює атом в йон, а не на новий хімічний елемент. Виліт ж електрона з ядра змінює заряд ядра (збільшує його) на одиницю. Спонтанне перетворення одних ядер в інші, яке супроводжується випромінюванням різних частинок, отримало назву радіоактивність.
Перетворення ядер відбуваються за так званим правилом зміщення, яке вперше сформулював Содді: під час а-розпаду ядро втрачає позитивний заряд 2е і маса його зменшується приблизно на чотири одиниці атомної маси. Отже, елемент зміщується на дві клітинки до початку Періодичної таблиці елементів Д. І. Менделєєва.
Символічно це можна записати так:
У випадку β-розпаду з ядра вилітає електрон. Тому заряд ядра збільшується на одиницю, а маса залишається майже незмінною:

Мал. 208
Після β-розпаду елемент зміщується на одну клітинку ближче до кінця Періодичної таблиці елементів Д. І. Менделєєва. Під час γ-випромінювання не відбувається зміни заряду; маса ж ядра змінюється надзвичайно мало.
Правила зміщення показують, що під час радіоактивного розпаду зберігається електричний заряд і наближено зберігається відносна атомна маса ядер.
Нові ядра, що утворюються під час радіоактивного розпаду, звичайно, також є радіоактивними.
Досліджуючи перетворення радіоактивних речовин, Резерфорд експериментально встановив, що їх активність з часом зменшується. Так, активність радону зменшується в два рази вже через 1 хв. Активність таких елементів, як Уран, Торій і Радій, також з часом зменшується, але значно повільніше. Для кожної радіоактивної речовини є певний інтервал часу, протягом якого активність зменшується у два рази. Цей інтервал називається періодом піврозпаду.
Період піврозпаду Т — це той час, за який розпадається половина всієї кількості наявних радіоактивних атомів.
Адже зменшення активності препарату в два рази можна досягти простим поділом його на дві рівні частини.
Графік спаду активності, тобто кількості розпадів за секунду, залежно від часу для однієї з активних речовин наведено на мал. 208, період піврозпаду цієї речовини — 5 діб.
Знайдемо тепер математичну формулу закону радіоактивного розпаду. Нехай кількість радіоактивних атомів у початковий момент часу (t - 0) дорівнює N0. Тоді по закінченні періоду піврозпаду їх кількість дорівнюватиме N0/2, а ще через один такий інтервал часу їх кількість становитиме:
Через інтервал часу t = nТ, тобто через n періодів піврозпаду Т, радіоактивних атомів залишиться

Оскільки  то
то 
Це і є основний закон радіоактивного розпаду.
За формулою знаходять кількість атомів, які ще не розпались, для будь-якого моменту часу.
знаходять кількість атомів, які ще не розпались, для будь-якого моменту часу.
Період піврозпаду — основна величина, що характеризує швидкість радіоактивного розпаду. Чим менший період піврозпаду, тим менший час життя атомів, тим швидше відбувається розпад. Для різних речовин значення його дуже розрізняються. Так, для урану 239/92U Т ~ 4,5 млрд років. Саме через це активність урану за кілька років помітно не змінюється. Для радію Т = 1600 років. Тому активність радію значно більша, ніж урану. Чим менший період піврозпаду, тим інтенсивніше відбувається розпад. Є радіоактивні елементи, в яких період піврозпаду становить мільйонні частки секунди.
Закон радіоактивного розпаду — це статистичний закон. Він справджується в середньому для великої кількості частинок.
Домашнє завдання : продивитись відео , написати конспект з даної теми.
Дата уроку :15.04.20
Тема уроку: Розв"язування задач.
Дата уроку :14.04.20
Тема уроку: Протонно - нейтронна модель атомного ядра. Ядерні сили . Енергія зв"язку атомних ядер.
Відкриття у 1896 р. французьким фізиком А. Беккерелем природної радіоактивності солей урану та подальше дослідження цього явища П. Кюрі і М. Склодовською-Кюрі поклали початок розвитку ядерної фізики. Загалом цей розділ фізики вивчає структуру атомного ядра, процеси радіоактивного розпаду і механізми ядерних реакцій. Інколи сюди відносять також фізику елементарних частинок.
Для ядерної фізики характерні відстані, сумірні з розміром ядра (~ 10-15 м), та енергії від мегаелектрон-вольт (МеВ) до гігаелектрон-вольт(ГеВ)
СКЛАД АТОМНИХ ЯДЕР
Досліди Е. Резерфорда, які утвердили ядерну модель атома, показали, що практично вся маса атома зосереджена в його ядрі, який має позитивний заряд. Подальші його дослідження взаємодії альфа-частинок з атомами Нітрогену увінчалися відкриттям протона — другої елементарної частинки, відкритої після електрона.
Вивчення властивостей протона показало, що він має позитивний заряд, який чисельно дорівнює заряду електрона е = 1,602 • 10-19 Кл; його маса значно більша: mр = 1,6726485 • 10-27 кг. Оскільки в ядерній фізиці прийнято користуватися атомною одиницею маси (а.о.м.) та її енергетичним еквівалентом — електрон-вольтом (еВ), маса спокою протона дорівнює mp = 1,007276470 а. о. м., що відповідає 938,2796 МеВ.
Протон (від грец. рг>tos — перший) — елементарна частинка, що є ядром атома Гідрогену; має позитивний заряд, що чисельно дорівнює заряду електрона
Відкриття на початку XX ст. ізотопів засвідчило, що їхні атомні маси кратні масі ядра атома Гідрогену. Тому Е. Резерфорд припустив, що ядра всіх хімічних елементів складаються із протонів. Протонно-електронна модель атома добре узгоджувалася з експериментальними даними щодо властивостей Гідрогену. Проте вона зіткнулася з низкою труднощів у поясненні будови ядер важчих хімічних елементів. Тому він висунув припущення про існування нейтронів — елементарних частинок, які також входять до складу ядра.
У 1932 р. англійський фізик Дж. Чедвік, досліджуючи властивості випромінювання, яке виникає під час бомбардування Берилію альфа-частинками, встановив, що це потік нейтральних частинок, маса яких приблизно дорівнює масі протона. Вимірювання показали, що маса спокою нейтрона mn = = 1,6749543 • 10-27 кг= 1,008665012 а.о.м., що відповідає 939,5731 МеВ.
Ізотопи (від грец. isos — однаковий і topos — місце) — різновиди одного й того самого хімічного елемента, що відрізняються за атомними масами
Нейтрон (від лат. пеШгит — ні те, ні інше) — нестабільна електрично нейтральна, тобто така, що не має ні позитивного, ні негативного заряду, елементарна частинка
У сучасній фізиці протони і нейтрони в ядрі називають нуклонами (від лат. шкіеш — ядро)
Число нуклонів у ядрі атома дорівнює його масовому числу А. Число протонів у ядрі атома дорівнює заряду ядра 2. Число нейтронів N = А-Z
У тому ж році радянський вчений Д. Д. Іваненко (українець за походженням, народився в Полтаві) і німецький фізик В. Гейзенберг незалежно один від одного запропонували оболонкову протонно-нейтронну модель ядра атома. Вони припустили, що атомне ядро складається з нуклонів — протонів і нейтронів, які розміщуються певними групами й утворюють ядерні оболонки. Кожен нуклон перебуває в певному квантовому стані, який характеризується енергією та набором інших квантових величин.
Згідно з цією моделлю, загальне число нуклонів, тобто сума протонів і нейтронів у ядрі атома, дорівнює масовому числу атома А; число протонів дорівнює заряду ядра атома Z, число нейтронів N = А — Z. В ядерній фізиці ізотоп хімічного елемента X прийнято позначати відповідним символом із зазначенням його масового числа А (зліва вгорі) і зарядового числа Z (зліва внизу), тобто у вигляді AZХ. Наприклад, найлегший ізотоп Гідрогену — протій, ядро якого складається з одного протона, позначають 11Н, альфа-частинку, що є ядром атома Гелію, 42Не тощо.
Заповнення ядерних оболонок підлягає певній закономірності — принципу Паулі: два тотожні нуклони не можуть одночасно перебувати в однаковому квантовому стані, тобто характеризуватися одним і тим самим набором квантових чисел. Тому існує ряд чисел — 2, 8, 20, 28, 40, 50, 82, 126, названих магічними, які визначають максимальне число нуклонів у заповнених оболонках.
Перехід ядра атома з одного стану в інший, наприклад із стабільного у збуджений чи навпаки, за оболонковою моделлю пояснюють як квантовий перехід нуклона з однієї оболонки на іншу. Щоразу, коли число протонів чи нейтронів стає магічним, відбувається стрибкоподібна зміна величин, які характеризують властивості ядра. Цим, зокрема, пояснюють фізичну причину існування періодичності у властивостях хімічних елементів, відображену періодичною системою Д. І. Менделєєва.
Принцип Паулі спочатку був сфор мульований для пояснення зако номірностей у заповненні елект-ронних орбіталей в атомі; згодом він був поширений на всі елемен тарні частинки з напівцілим спіном
Принцип Паулі є фізичною суттю періодичного закону Д. І. Менделєєва
Оболонкова модель атомного ядра є однією з найпродуктивніших у ядерній фізиці, зокрема в поясненні періодичності власти-востей ядер і механізму ядерних реакцій. Проте вона також має свої обмеження, оскільки неспроможна розтлумачити властивості важких ядер і пояснити всі типи взаємодії нуклонів у ядрі. Тому існують також інші моделі атомних ядер, наприклад, крапельна, згідно з якою атомне ядро уявляють у формі краплі особливої квантової рідини.
ЯДЕРНІ СИЛИ ТА ЕНЕРГІЯ ЗВ'ЯЗКУ АТОМНИХ ЯДЕР
Нуклони в ядрі атома утримуються завдяки ядерним силам, які є проявом однієї з чотирьох фундаментальних взаємодій — сильної взаємодії. За своєю природою вони короткодіючі (г~ 10-15 м), але дуже інтенсивні. У межах атомного ядра вони майже у 100 разів переважають сили електростатичної взаємодії двох протонів і в 1038 разів — силу їхньої гравітаційної взаємодії. Проте на відстанях, більших за розміри ядер, вони настільки малі, що їхньою дією можна знехтувати.
Ядерні сили діють незалежно від наявності в нуклонах електричного заряду. Внаслідок цього в атомному ядрі утримуються електронейтральні нейтрони і не розлітаються однойменно заряджені протони. Експериментальні дослідження сил ядерної взаємодії протон-протонних, протон-нейтронних і нейтрон-нейтронних пар показали, що в усіх випадках вони однакові і не залежать від типу нуклона.
Ядерні сили — короткодіючі, оскільки проявляють себе на відстанях у межах атомного ядра (10-15 м)
Обмінний характер ядерної взаємодії подібний до ковалентного зв'язку між атомами в молекулі, де роль такого «посередника» відіграють валентні електрони
У 1935 р. японський фізик X. Юкава висунув припущення, що природа ядерних сил полягає в їхньому обмінному характері, тобто, за його передбаченням, наявність ядерних сил зумовлює гіпотетична частинка ненульової маси, якою обмінюються між собою нуклони під час взаємодії.
Пізніше, у 1947 р. така частинка була експериментально виявлена і названа пі-мезоном. Встановлено, що залежно від типу взаємодіючої пари нуклонів (протон—протон, нейтрон—нейтрон, протон—нейтрон, нейтрон—протон) існує три види пі-мезонів: позитивний (п+), негативний (п-) і нейтральний (п0). Перші два мають масу спокою, яка дорівнює 274 масам електрона те, що відповідає приблизно 140 МеВ; маса спокою третього дорівнює 264 те, що відповідає приблизно 135 МеВ.
Пі-мезони не входять до складу протонів і нейтронів. Вони лише виявляють себе в ядерній взаємодії як обмінні частинки, завдяки яким відбувається сильна взаємодія в атомному ядрі. Ця взаємодія є чинником об'єднання нуклонів у стабільне атомне ядро. Зв 'язаний стан нуклонів у ядрі характеризується енергією зв'язку, яка витрачається на те, щоб утримувати протони і нейтрони у такому стані. Тобто це енергія, потрібна для виконання роботи проти дії ядерних сил, що утримують нуклони в ядрі у зв'язаному стані.
Якщо порівняти масу атомних ядер із сумою мас нуклонів, які їх складають, то з'ясується, що вони не збігаються: маса ядра завжди менша за масу її складових. Тому кажуть, що існує дефект мас Δm, який визначається різницею суми мас Z протонів і N нейтронів та маси ядра mя:
Пі-мезони — це кванти ядерного поля, подібні до фотонів, які є квантами електромагнітного поля
Пі-мезони інколи називають піонами
Енергія зв'язку ядра атома — це та мінімальна енергія, яку треба затратити, щоб роз'єднати ядро на окремі нуклони, що входять до його складу
Точні вимірювання мас атомних ядер показали, що тя < Zтр + Nтп
Причина виникнення дефекту мас полягає в тому, що для утворення ядра з вільних протонів і нейтронів потрібно виконати роботу, яка чисельно дорівнює енергії зв'язку. Отже, дефект мас визначає енергію зв'язку ядра. Взявши до уваги формулу взаємозв'язку маси та енергії, отримаємо:
Природно, що енергія зв'язку різних ядер може бути різною. Проте якщо віднести її до числа нуклонів, то спостерігається певна іалежність питомої енергії зв'язку нуклона в ядрі від масового числа атома А (мал. 8.1).
Розглянемо графік такої залежності. Спочатку крива різко зростає і досягає максимуму 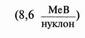 в ізотопів елементів з нуклон масовим числом від 50 до 60 (Ферум і близькі до нього елементи).
в ізотопів елементів з нуклон масовим числом від 50 до 60 (Ферум і близькі до нього елементи).
У міру подальшого збільшення масового числа атома крива починає плавно спадати, посягаючи значення 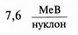 в Урану 23892U. Такий вигляд кривої зумовлений закономірностями забудови ядерних оболонок протонами і нейтронами. Проте оболонкова модель ядра неспроможна пояснити характер забудови всіх елементів. Зокрема, вона непридатна для важких елементів, де істотними стають електростатичні сили взаємодії протонів.
в Урану 23892U. Такий вигляд кривої зумовлений закономірностями забудови ядерних оболонок протонами і нейтронами. Проте оболонкова модель ядра неспроможна пояснити характер забудови всіх елементів. Зокрема, вона непридатна для важких елементів, де істотними стають електростатичні сили взаємодії протонів.
Домашнє завдання: зробити конспект та дати відповіді на тести.
Дата уроку : 13.04.20
Тема уроку: Квантово - оптичні генератори ( лазери).
Завдання : підготувати цікаві факти з даної теми ( доповідь)!!!
Дата уроку : 08.04.20
Тема уроку: Види спектрів.Основи спектрального аналізу.
Переглянути відео :
Ми знаємо, що спектральний склад світла вивчають за допомогою спектральних апаратів. Що ми можемо дізнатися про тіло завдяки його спектральному аналізу?
1. Лінійчасті спектри
Якщо кинути дрібочку кухонної солі в полум’я газового пальника, воно забарвлюється в жовтий колір.
Проблемні питання
• Яка причина цього явища?
До складу кухонної солі входить Натрій, і саме атоми цього елемента зумовлюють характерне жовте випромінювання.
• Який механізм появи цього випромінювання?
У полум’ї пальника натрій нагрівається, і атоми Натрію переходять у збуджений стан. Повертаючись в основний стан, атоми випромінюють електромагнітні хвилі, причому відповідно до постулатів Бора – чітко визначених частот, а отже, і довжин. Для Натрію найбільша інтенсивність випромінювання припадає на довжини хвиль, які відповідають світлу жовтого кольору. Численні дослідження довели, що за нагрівання до дуже високої температури атоми будь-якого хімічного елемента можуть випромінювати світло, вузький пучок якого розкладається призмою на кілька пучків.
Лінійчастий спектр випромінювання –це різнокольорові лінії, розділені широкими темними смугами.
Такі спектри дають речовини в газоподібному атомарному (не молекулярному) стані за високої температури.
Лінійчастий спектр поглинання – це темні лінії на фоні неперервного спектра. Спостерігається коли біле світло пропускають через речовину в газоподібному стані. Розташування темних ліній у спектрі поглинання речовини за даної температури точно збігаються з розташуванням світлих ліній у спектрі випромінювання цієї самої речовини за тієї самої температури. Речовина в атомарному газуватому стані за даної температури випускає і поглинає хвилі однакових частот (правило Кірхгофа).
Лінійчастий спектр будь-якого конкретного хімічного елемента не збігається з лінійчастим спектром інших хімічних елементів, а отже, є своєрідною «візитівкою» елемента.
Смугастий спектр випромінювання – це система смуг із численних і дуже близько розташованих одна до одної ліній.
Такі спектри утворюються молекулами, що слабо зв`язані або зовсім не зв`зані між собою. Така спектральна картина пояснюється тим, що при збудженні молекули відбуваються як енергетичні переходи в атомах (атоми переходять у стани з більшим рівнем енергії), так і збудження коливань атомів усередині молекули й обертання молекули. Енергія коливального руху атомів усередині молекули та енергія обертального руху молекули теж підпорядковуються законам квантової фізики і мають низку дискретних значень. Таким чином, один енергетичний рівень розбивається на безліч коливальних підрівнів. Кількість можливих переходів (повернень в основний стан) різко збільшується, що зумовлює виникнення величезної кількості ліній спектра, які зливаються в широкі смуги.
Неперервний спектр випромінювання –це спектр, в якому представлені всі довжини хвиль від червоного до фіолетового.
Неперервний спектр випромінюють стиснені гази, рідини і тверді тіла нагріті до високої температури. Існування неперервного спектра зумовлене не тільки властивостями окремих випромінюючих атомів, а й значно залежить від взаємодії атомів між собою.
2. Основи спектрального аналізу
Спектральний аналіз – це метод якісного і кількісного визначення складу речовини за її спектром.
Дослідження спектрів випромінювання дозволяє одержати інформацію про елементний склад речовин. Зараз визначено спектри всіх атомів й складено таблиці спектрів. Дослідження спектрів поглинання зір та інших астрономічних об’єктів дозволяє дізнатися про їх хімічний склад, температуру, тиск, швидкість та інші важливі параметри. Якщо сфотографувати спектр сонячного світла, отриманий за допомогою якісного спектроскопа, то на знімку будуть спостерігатися чіткі лінії поглинання. Уперше ці лінії описав німецький фізик Йозеф Фраунгофер (1787-1826), тому вони отримали назву – лінії Фраунгофера. Поява цих ліній пов’язана з проходженням сонячного світла через атмосферу Сонця і частково з проходженням через атмосферу Землі. Таким чином, лінії Фраунгофера – це спектр поглинання. За цими лініями було встановлено, що на Сонці є Гідроген, Кальцій, Натрій, Ферум та інші хімічні елемент
Д/З.Зробити конспект та пройти тест з даної теми на сайті На урок.
Зробити скрін тесту та надіслати мені особисто!.
Дата уроку : 07.04.20
Тема уроку: Розв"язування задач.
Повторити конспект , опрацювати задачі запропоновані у відео.
Виконати завдання на онлайн платформі:
Дата уроку : 06.04.20
Тема уроку: Дослід Резерфорда. Постулати Бора.
Енергетичні рівні атома.
1. Модель атома Томсона. До 1902року було здійснено достатньо експериментів, які переконливо довели, що електрон є однією з основних складових частий будь-якої речовини.
Дж. Дж. Томсон показав на основі класичної електромагнітної теорії, що розміри електрона мають бути порядку 10-15 м. Крім того, було відомо, що розміри атома становлять кілька ангстрем (один ангстрем дорівнює 10-10 м). На цій підставі Томсон 1903 року запропонував свою модель атома, відповідно до якої атоми являють собою однорідні кулі з позитивно зарядженої речовини, у якій містяться електрони (рис. 142). Сумарний заряд електронів дорівнює позитивному зарядові атома. Тому атом у цілому електрично нейтральний.
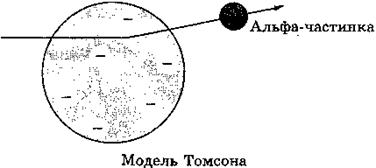
Рис. 142
Ця модель дістала назву «пудинг», оскільки електрони були вкраплені в позитивно заряджене середовище, немов ізюм у пудинг.
Відхилення електрона в атомі від положення рівноваги приводить до виникнення повертаючої сили. А отже, електрон, виведений яким-небудь способом із положення рівноваги, здійснює коливання й тому є джерелом електромагнітного випромінювання.
Модель Томсона здавалася привабливою з тієї точки зору, що передбачала наявність електронів в атомі. Однак вона проіснувала тільки до 1911 року.
2. Досліди Резерфорда.У 1911році Е. Резерфорд запропонував своїм співробітникам (жсперимеїггально перевірити переконливість моделі атома Томсона. Ідея досліду була проста. Якщо модель атома Томсона відповідає дійсності, то експериментатори, пропускаючи крізь дуже тонку металеву плівку вузький пучок швидких α -частинок, не повинні виявити скільки-небудь помітного відхилення цих частинок.
Резерфорд установив, що кожна α-частинка, потрапляючи на екран із сірчистого цинку, викликає спалах світла. Зазнавши розсіювання в золотій фользі, α -частинки вдарялися потім в екран і реєструвалися за допомогою мікроскопа.
Очікувалося, що пучок α -частинок під час проходження крізь тонку фольгу злегка розсіюється на невеликі кути. Це дійсно спостерігалося. Але несподівано з'ясувалося, що приблизно одна α -частинка з 20 000,які падають на золоту фольгу завтовшки усього лише 4 · 10-5 см, повертається назад у бік джерела.
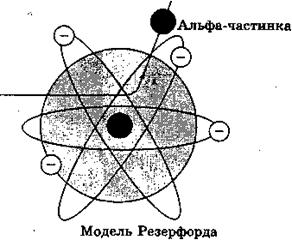
Рис. 143
Резерфордові знадобилося кілька років, щоб остаточно зрозуміти таке несподіване розсіювання а-частинок на великі кути. Він дійшов висновку, що позитивний заряд атома зосереджений у дуже малому об'ємі в центрі атома, а не розподілений по всьому атому, як у моделі Томсона.
3. Ядерна модель атома Резерфорда.Резерфорд запропонував ядерну («планетарну») модель атома:
1)атоми будь-якого елемента складаються з позитивно зарядженої частинки, що дістала назву ядра;
2)до складу ядра входять позитивно заряджені елементарні частинки — протони (пізніше було встановлено, що й нейтральні нейтрони);
3)навколо ядра рухаються електрони, що утворюють так звану електронну оболонку.
Користуючись схемою (рис. 143), можна пояснити спочатку будову атома Гідрогену, що має тільки один протон і один електрон. Потім розглядаємо ядерну модель будови більш складних атомів — Гелію й Літію. Як вправа може бути розглянута будова атомів низки більш складних елементів.
Необхідно зазначити, що атом, який утратив (чи набув) один або кілька електронів, уже не буде нейтральним, а матиме позитивний (або негативний) заряд. Його називають позитивним (або негативним) іоном.
4. Непереконливість класичної теорії в поясненні випромінювання та поглинання енергії атомом.За всієї переконливості планетарної моделі виникла ціла низка нездоланних перешкод під час пояснення будови атома. Відповідно до класичної теорії, система, що складається з масивного позитивно зарядженого ядра та легких, негативно заряджених електронів, буде стійкою тільки в тому випадку, коли електрони перебувають у русі. Таким чином, атом має бути подібний до мініатюрної Сонячної системи, у якій роль Сонця відіграє ядро, а планет — електрони.
Аналогія була б досить повною (адже електричні й гравітаційні сили залежать від відстані, як 1/r2), якби не один прогноз класичної теорії. Відповідно до нього електричні заряди, які прискорено рухаються, мають випромінювати енергію у вигляді електромагнітних хвиль. Тому електрони, які рухаються по «планетарних» орбітах, мали б шляхом випромінювання втрачати енергію руху й у результаті швидко наближатися до ядра. Розрахунки показували, що електрон в атомі Гідрогену мав би випроменити всю свою енергію за малу частку секунди. Однак в атомі цього не стається.
Більш того, спектральні лінії, відповідно до класичних уявлейь, не повинні існувати, а має бути тільки неперервний спектр.
Отже, на початку XX століття серед довжелезної низки нерозв'язаних проблем фізики атома однією з найбільш гострих було пояснення оптичних спектрів атома. Теорія атома мала визначити положення кожної спектральної лінії в спектрах усіх елементів.
У 1885 році швейцарський фізик І. Бальмер довів, що всі частоти видимої частини спектра випромінювання атома Гідрогену можуть бути обчислені за дуже простою формулою (серія Бальмера):
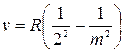 ,
,
де-R — величина стала, а m = 3, 4, 5, ..., ∞.
Пізніше, 1906 року, англійським фізиком Лайманом була відкрита серія ліній в ультрафіолетовій частині спектра Гідрогену (серія Лаймана):
 .
.
У 1908 році німецьким фізиком Пашеном була відкрита серія ліній в інфрачервоній частині спектра Гідрогену (серія Пашена):
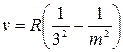 .
.
Отже, частоту будь-якої лінії в спектрі атома Гідрогену можна подати у вигляді:
 .
.
Із цієї формули видно, що в спектральних закономірностях особливо важливу роль відіграють цілі числа т і п, так звані головні квантові числа.
Усі наведені вище формули є чисто емпіричними. Пояснити лінійчастий спектр випромінювання атомів Гідрогену вдалося лише після створення 1913 року Н. Бором квантової теорії будови атома Гідрогену.
5. Квантові постулати Бора.В основі теорії Бора лежать такі положення:
• у стійкому атомі електрон може рухатися лише по особливих, стаціонарних орбітах, не випромінюючи при цьому електромагнітної енергії;
• атом може переходити з одного стаціонарного стану до іншого. Під час переходу атома зі стаціонарного стану з більшою енергією до стану з меншою енергією атом випромінює квант енергії, якому відповідає частота
 ;
;
• у стаціонарному стані атома електрон, рухаючись по коловій орбіті, повинен мати дискретні, квантові значення моменту імпульсу 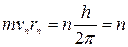 ħ, де п = 1 , 2, 3 — номер орбіти; r — радіус орбіти:
ħ, де п = 1 , 2, 3 — номер орбіти; r — радіус орбіти:
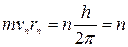 ħ, де п = 1 , 2, 3 — номер орбіти; r — радіус орбіти:
ħ, де п = 1 , 2, 3 — номер орбіти; r — радіус орбіти: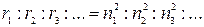 .
.
Постулати Бора пояснюють походження лінійчастих спектрів і їх закономірності.
Перший постулат називається постулатом стаціонарних станів.Цей постулат суперечить класичній механіці та електродинаміці Максвелла.
Другий постулат називається правилом частот.Якщо електрон перескакує на іншу орбіту, де його енергія менша, то куди дівається надлишок енергії? Адже зникнути, перетворитися на ніщо енергія не може. «Шукайте її поза атомом!» — заявляє Бор. Вона виділяється з атома у вигляді кванта світлової енергії (поняття про який було уведено Планком), а електрон, який випроменив, рухається по орбіті, тепер вже іншій, і знову не випромінює.
Третій постулат називається правилом квантування орбіт.Виявилося, що можна одержати низку дискретних розділених стаціонарних станів тільки за того припущення, що момент імпульсу електрона квантується. Звідси дістаємо вираз для радіусів орбіт:
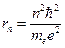 ,
,
де те й е — маса та заряд електрона.
Фізики до появи теорії Бора не могли розшифрувати складні спектри. Коли ж Бор довів, що «спектр — це біографія атомів, точніше атомних електронів», учені змогли, комбінуючи різні орбіти електронів в атомі, обчислити всі лінії, що спостерігаються у спектрі. Таким чином, джерелом світла є збуджений атом, світло генерується під час переходу атома з одного збудженого стану в інший, частота світла, що генерується, пропорційна ΔЕ, світло випромінюється й поглинається у вигляді квантів.
Слід звернути увагу учнів на половинчастість теорії Бора, її внутрішню суперечливість. У ній поряд із законами класичної фізики (закони Ньютона й Кулона, формули кінетичної й потенціальної енергій) уводяться квантові постулати, які зовсім не випливають із законів класичної фізики. Тому теорія Вора змогла пояснити закономірності будови тільки найпростішого атома — атома Гідрогену. Пояснити ж закономірності будови складних атомів вдалося тільки після створення більш послідовної теорії — квантової механіки й квантової електродинаміки.
6.Експериментальне підтвердження постулатів Бора.Ідеї Н.Бора були підтверджені експериментально 1913року в досліді Д. Франка та Г. Герца. Ідея цього досліду полягала у вимірюванні кількості енергії, що передається атомом під час зіткнення з електроном.
Із досліду Франка й Герца випливає, що енергія атома може мати лише дискретні значення Е1, Е2, Е3, ..., Еп , де Е1 — енергія нормального (не-збудженого) стану атома.
7.Енергія атома Гідрогену.Повну енергію атома Е можна подати у вигляді суми кінетичних енергій електрона й атомного ядра та потенціальної енергії їх взаємодії. Будемо вважати ядро нерухомим. Тоді в енергію атома ввійде тільки кінетична енергія електрона 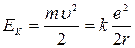 і потенціальна енергія кулонівської взаємодії
і потенціальна енергія кулонівської взаємодії 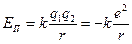 .
.
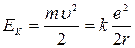 і потенціальна енергія кулонівської взаємодії
і потенціальна енергія кулонівської взаємодії 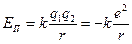 .
.
Таким чином 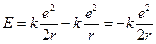 .
.
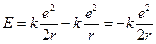 .
.
Ми бачимо, що енергія атома від'ємна й зі збільшенням радіуса орбіти r зростає. Визначимо радіус орбіти в атомі Гідрогену.
Оскільки кулонівська сила надає електронові доцентрового прискорення а = υ2r, то за другим законом Ньютона  .
.
 .
.
Із третього постулату Бора mυnrn = nħ швидкість, з якою рухається електрон по орбіті, дорівнює 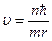 . Застосовуючи ці формули, дістаємо радіус орбіти:
. Застосовуючи ці формули, дістаємо радіус орбіти: 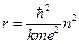 .
.
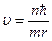 . Застосовуючи ці формули, дістаємо радіус орбіти:
. Застосовуючи ці формули, дістаємо радіус орбіти: 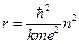 .
.
Здобута формула показує, що радіуси стаціонарних орбіт мають дискретні значення, пропорційні квадратові цілого числа п. В основному (не-збудженому) стані (п = 1) атом має мінімальні розміри r1 = 0,53·10-10 м. Підчас переходу атома в збуджені стани (п = 2, 3,...) його радіус збільшується за законом r = r1п2.
Підставляючи вираз для радіуса орбіти до формули для енергії, остаточно дістаємо:
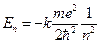 .
.
Повна енергія атома є величиною від'ємною, і тільки у разі іонізації повна енергія атома дорівнює нулю. Це рівносильно твердженню: у нормальному стані атом має мінімальну енергію, а у разі іонізації — максимум, енергії, яка дорівнює нулю.
Для атома Гідрогену енергія іонізації дорівнює 13,6 еВ. Оскільки 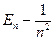 , то
, то 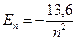 .
.
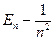 , то
, то 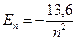 .
.
Для незбудженого стану при п = 1 Е1 = -13,6 еВ; при п = 2 Е2 = -3,4еВ; при n = 3E3 =-1,5еВ; при п = ∞ Е = 0.
8. Спектр випромінювання атома Гідрогену.Відповідно до другого постулату Бора, випромінювання відбувається під час переходу атома з верхніх енергетичних рівнів на нижні.
Випромінювані при цьому фотони будуть мати частоти, які визначаються формулою: 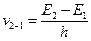 .
.
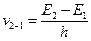 .
.
Переходи в перший збуджений стан із верхніх рівнів утворюють серію Бальмера, що спостерігається у видимому світлі. На рис. 144 показані серії випромінювання атома Гідрогену в різних діапазонах.
Під час випускання світла атом може переходити з будь-якого стану в незбуджений відразу, наприклад, Е5 – Е1, = hv5,1, або послідовно, через проміжні стани:
E5 - E4 = hv5, 4
E4 - E3 = hv4, 3
E3 - E2 = hv3, 2
E2 – E1 = hv2, 1
Усі ці переходи здійснюються відповідно до закону збереження й перетворення енергії: hv5, 1 = hv5, 4 + hv4, 3 + hv3, 2 + hv2, 1.
Домашнє завдання. Підготовити конспект з даної теми та вивчити його.
Дата уроку : 01.04.20
Тема уроку: Захист навчальних проектів з теми :"Оптика".
Любі друзі! Чекаю на ваші звіти з даного проекту, дякую!!!
Дата уроку : 31.03.20
Тема уроку : Навчальний проект з теми :"Оптика".
Пропоную вам теми з яких ви можете вибрати!
- Багатоярусне вирощування рослин за допомогою відбитого сонячного світла.
- Вивчення властивостей зображень, що отримуються за допомогою збираючої лінзи.
- Виготовлення приладів для спостереження інтерференції і дифракції світла.
- Визначення жирності молока методом розсіяння світлового променя на жирових кульках.
- Використання сонячної енергії.
- Вимір довжин світлової хвилі усього спектру.
- Вимір коефіцієнта пульсації ламп освітлення при роботі з ПЕОМ.
- Відображення предметів в дзеркалах.
- Відображення світла очима кішки.
- Відображення світла. Перископ і його застосування.
- Вклад М.В. Ломоносова у винахід і удосконалення оптичних приладів.
- Вплив зовнішніх чинників на зір школяра.
- Вплив різних ділянок спектру видимого світла на швидкість зростання рослин.
- Вплив сонячного світла на зростання рослин.
- Дисперсія світла.
- Дослідження властивостей світла.
- Дослідження модуляції випромінювання світлодіодів і напівпровідникового лазера.
- Дослідження штучних джерел світла, вживаних в школі.
- Дослідний зразок сонячної батареї із застарілих кремнієвих транзисторів і діодів.
- Загадки полярних сяйв
- Загадки увігнутих дзеркал.
- Залежність відбивних здібностей матеріалу від його кольору.
- Залежність ростових процесів у рослин від якості світла.
- Захід як фізичне явище.
- Зір в століття технічного прогресу.
- Зір у сучасному світі.
- Зорові ілюзії
- Ілюзії і парадокси зору, або обмани, викликані прагненням до істини.
- Ілюзія, міраж або парадокси зору.
- Інфрачервоне випромінювання і його деякі властивості.
- Легенда або бувальщина "Промені Архімеда"?
- Лінзи.
- Люмінесценція.
- Майбутнє за світлодіодами.
- Моріус Корнеліус Ешер. Інструменти обману.
- Нове покоління освітлювальних ламп.
- Оптика і образотворче мистецтво.
- Оптика. Світло
- Оптика. Телескоп.
- Оптична система ока.
- Оптичне мистецтво (оп-арт) як синтез науки і мистецтва.
- Оптичні ілюзії
- Оптичні ілюзії або обман зору.
- Оптичні ілюзії і отримання стереоскопічних зображень.
- Оптичні прилади і їх застосування в медицині.
- Оптичні прилади, винайдені і вдосконалені М.В. Ломоносовим.
- Оптичні системи
- Оптичні явища в природі
- Оптичні явища навколо нас
- Особливості поширення світла
- Отримання веселки в домашніх умовах.
- Оцінка значення швидкості світла в речовині.
- Полярне сяйво
- Світло і його властивості
- Світло і колір в природі
- Світлові явища навколо нас
- Світлодіоди - сучасні джерела світла.
- Технічне застосування лінз
- У світі дзеркальних поверхонь.
- У світі мильних бульбашок
- У світі поляризованого світла.
- Формування світлових візерунків за допомогою світлодіодних випромінювачів.
- Хемілюмінесценція
- Хімічна історія дзеркал.
- Як відбивається світло?
Чекаю фаші фото звіти на наступний урок, коли у нас буде захист даних проектів!
Дата уроку : 30.03.20
Тема уроку : Контрольна робота з теми : Оптика
Варіант №1
1. (1б.) Що таке квант світла? Назвіть властивості квантів.
2. (1б.) Запишіть формулу для знаходження тиску світла
3. (1б.) Сформулюйте закони фотоефекту
4. (1б.) Запишіть рівняння Ейнштейна для зовнішнього фотоефекту
5. (1,5 б.) Що називають червоною межею фотоефекту? Чи залежить вона від міри освітленості матеріалу?
6. (1,5 б.) Як Ви розумієте поняття «корпускулярно-хвильовий дуалізм»
7. (2б.) Потік монохроматичного світла λ =5*10-7
8. (2б.) Чи відбудеться фотоефект уразі опромінення цинкової пластинки ультрафіолетовим світлом довжиною хвилі 400 нм? Яку максимальну швидкість можуть мати фотоелектрони при цьому? Робота виходу електрона для цинку 8,48 еВ?
9. (2б.) У якого металу – цезію чи вольфраму – червона межа фотоефекту вища? Роботи виходу цих металів дорівнюють відповідно, 1,8 та 4,54 еВ?
Варіант №2
1. (1б.) Що таке фотоефект?
2. (1б.) Запишіть формулу для обчислення енергії кванта
3. (1б.) Сформулюйте закони фотоефекту
4. (1б.) Застосування фотоефекту. Наведіть приклади.
5. (1,5 б.) Що називають червоною межею фотоефекту? Чи залежить вона від міри освітленості матеріалу?
6. (1,5 б.) Як Ви розумієте поняття «корпускулярно-хвильовий дуалізм»
7. (2б.) Який імпульс фотона, енергія якого дорівнює 6*10-19 Дж?
8. (2б.) У якого металу – цезію чи вольфраму – червона межа фотоефекту вища? Роботи виходу цих металів дорівнюють відповідно, 1,8 та 4,54 еВ?
9. (2б.) Чи відбудеться фотоефект уразі опромінення цинкової пластинки ультрафіолетовим світлом довжиною хвилі 400 нм? Яку максимальну швидкість можуть мати фотоелектрони при цьому? Робота виходу електрона для цинку 8,48 еВ?







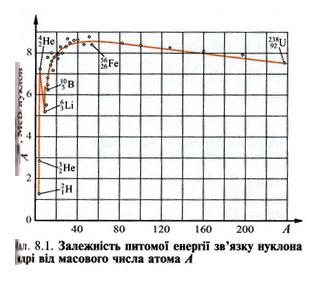


Немає коментарів:
Дописати коментар